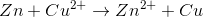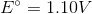例子问题
例子问题1:吉布斯自由能和自发性
假设某rxn∆H = -28 kJ,∆S= -60 J/K。在什么温度下
从自发变成非自发?
50
467 K
46.7 K
500 K
467 K
约467 k。∆G=∆H-T∆S,当∆G < 0时,自发出现rxn
且当∆G > 0时为非自发。因此,如果我们设∆G=0,并求解T的方程,我们会看到,当T=467K时,发生了从自发到非自发的交叉。
例子问题1:吉布斯自由能和自发性
如果反应商(Q)大于平衡常数(K),吉布斯自由能是什么?
它大于零。
它小于零。
需要更多的信息来确定吉布斯自由能。
它等于0。
它大于零。
如果Q大于K,则反应已超过平衡态。它将非自发地进行(因为已经达到平衡),这就意味着ΔG(吉布斯自由能)一定是正的,或者大于零。
例子问题3:吉布斯自由能和自发性
反应的熵和焓都是负的。反应是自发的吗?
反应是自发的当且仅当焓的大小大于熵的大小乘以温度
反应是自发的当且仅当焓的大小大于熵的大小
反应是自发的当且仅当熵的大小大于焓的大小乘以温度
反应是自发的
这种反应不是自发的
反应是自发的当且仅当焓的大小大于熵的大小乘以温度
如果反应的吉布自由能为负,则反应是自发的。
如果

问题4:吉布斯自由能和自发性
一个系统__________而且__________永远不会自发。
正焓。负熵
正焓。积极的熵
负焓。积极的熵
负焓。负熵
正焓。负熵
吉布自由能方程用于确定反应的自发性,其形式如下:



这意味着这些条件总是会导致非自发反应。
例子问题1:吉布斯自由能和自发性
考虑一下原电池中的以下反应:
如果下面关于反应的陈述是错误的呢?
反应是自发的
吉布自由能是正的
细胞电位是正的
平衡常数大于1
吉布自由能是正的
原电池由于自发反应而产生正的细胞电位。自发反应的吉布自由能总是负的。
平衡常数大于1表示生成物的平衡浓度大于反应物的平衡浓度,符合自发反应。
例子问题6:吉布斯自由能和自发性
考虑一下原电池中的以下反应:
标准条件下反应的吉布自由能是多少?
你可以用下面的公式求出原电池的吉布自由能:



我们已知常数值和细胞电位。转移的电子的摩尔数等于反应中原子电荷的变化量。在这个反应中,铜从电荷中还原
利用这些值,我们可以求出细胞的吉布自由能。
注意,这个值是负的。原电池是自发的,在标准条件下具有负的吉布自由能。
例子问题1:吉布斯自由能和自发性
如果反应商(Q)小于平衡常数(K),吉布斯自由能是什么?
我们必须知道反应焓才能确定答案
它大于零
我们必须知道反应温度才能确定答案
它小于零
它等于0
它小于零
如果Q小于K,那么反应还没有达到平衡态。它会自发地向前运动。由于它是自发地向前运动,这就意味着ΔG(吉布斯自由能)一定是负的,或者小于零。
在数学上计算吉布斯自由能时,焓和温度是必要的,但反应商和平衡常数提供了足够的信息来定性地确定反应是自发进行的。
例子问题1:吉布斯自由能和自发性
下列哪个反应只有在足够高的温度下才自发?
以上都不是
∆h -,∆s +
∆h +,∆s -
∆h -,∆s -
∆h +,∆s +
∆h +,∆s +
根据吉布斯自由能,∆G =∆H - T∆S,我们发现∆H -将有助于自发性(∆G<0)。由于我们关注的是温度,为了使∆S在高温下才发生非自发反应,∆H为正,∆S为正。
例子问题2:吉布斯自由能和自发性
如果一个反应的焓为正值熵为负值,下面哪个选项是正确的?
已知自由能方程(δ)G = (δ)H- t (δ)S,我们可以确定,如果H为正,S为负,反应在任何温度下都是非自发的。这种组合总是会导致一个正的G值,这意味着反应发生需要自由能,因此它是非自发的。
例子问题2:吉布斯自由能和自发性
自发过程中什么是正确的?
ΔG→0和K←Q
ΔG→0和K→Q
K⇌0
ΔG←0和K←Q
ΔG←0和K→Q
ΔG←0和K→Q
对于自发过程,自由能的变化一定是负的。此外,Q必须小于K这样反应才能向前进行,朝着平衡进行。