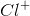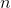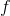例子问题
例子问题1:周期性规律
下面是一个经过修改的是非题。在它中,你必须决定每一个单独的陈述是否为真(T)或假(F)。如果两者都为真,那么你也必须决定第二个陈述是否是第一个陈述的正确解释(CE)。
I:碱土金属族原子的离子半径比原子半径小
因为
II:这类原子通常为了成为离子而失去电子,导致离子缺乏原子中存在的最外层能级。
T、F
T, T (II不是对I的正确解释)
T, T, CE
F T
F, F
T, T, CE
碱土金属是ⅱ族元素,如铍和镁。它们想要在最外层的能级上有一个完整的八隅体,所以它们倾向于失去两个电子来形成离子态,这给了它们惰性气体在前一个能级的电子构型,因此离子半径更小。因此,两个表述都是正确的,第二个表述正确地解释了第一个表述。
例子问题1:元素和原子
原子半径最小的元素通常出现在元素周期表的哪一部分?
左下角
左上角
右下角
右上角
内部过渡金属
右上角
由于新能级的增加,原子半径趋向于向下增加;然而,由于屏蔽的增加和核质量的增加,它会在一段时间内减少。由于这些原因,原子半径最小的元素会出现在元素周期表的右上角。
例子问题1:Sat化学科目测试
一个磷原子有15个质子,16个中子和15个电子。原子的质量数是多少?
质子和中子的质量都约为1amu,而电子的质量则可以忽略不计。因此,质量数等于质子数和中子数,即31。
例子问题1:Sat化学科目测试
下列哪一个具有电子构型![[Ne]3s^23p^6](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/1074018/gif.latex)
任务是找到前三个能级完全充满的原子或离子。氩不是一个答案选项,这意味着它必须是一个原子序数接近氩原子序数的离子。回想一下,带正电荷意味着电子从最外层失去,带负电荷意味着电子从最外层获得,唯一可行的答案是
例子问题2:Sat化学科目测试
下列哪个变量确定了有三个轨道的子能级?
的




例子问题1:Sat化学科目测试
根据VSEPR理论和电子构型,下面哪个分子是不与它正确的几何结构相匹配?




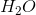


例子问题1:分子
分子的几何结构是什么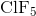
四面体
三角金字塔形
八面体
方形锥体
广场平面
方形锥体
里面有六个电子畴


例子问题1:化合物和分子
以下哪一个是正确的名字
五氧化二氮
一氧化氮
一氧化二氮
二氮tetraoxide
二氧化氮
二氮tetraoxide
为了回答这个问题,重要的是首先要确定发生了什么样的键,以便正确地命名分子。当氮和氧形成
因为形成了共价键,我们可以根据分子中每个原子的数量来确定分子的名称。生成的分子中有两个氮原子,所以名称中“氮”部分前面的前缀将是“二”,意思是两个.生成的分子中有四个氧原子,所以名称中“氧”部分的前缀是“tetra”,意思是“tetra”四个.
分子名称将按字母顺序排列,第二个原子将以“-ide”作为后缀。因此,正确答案是“四氧化二氮”。
例子问题1:化合物
钙离子和硫酸盐离子形成的化合物的分子式是什么?
为了正确回答这个问题,重要的是要有离子键的形成,多原子离子和元素周期表的知识。首先,重要的是要注意钙离子和硫酸盐离子会形成离子键。知道了这一点,就可以理解成价电子将在离子之间交换,因此,相互吸引的带相反电荷的离子将会形成。
钙在元素周期表的第二列,所以它会提供两个离子给硫酸盐多原子离子。这将形成钙离子(

一个钙离子提供两个电子,两个电子都被一个硫酸盐多原子离子接受,因此所用的钙离子与所用的硫酸盐多原子离子的比例为1:1。这意味着每一种离子中只需要一个离子就能形成化合物,形成分子式
一开始,可能很容易把公式写成
例子问题2:Sat化学科目测试
以下都是锌的性质。下列哪项是化学锌的性质?
A.锌放在酸里会产生氢气。
B.锌在
C.锌的密度是
D.锌是一种灰色金属。
E.锌在潮湿空气中腐蚀。
B和C
A, C和E
C
A和E
B
A和E
物质的物理性质是可以在不改变它的情况下观察和测量的方面。化学性质衡量发生化学变化的可能性。锌对酸和潮湿空气的反应都是化学性质,因为锌在每种环境中都在发生化学变化。锌的颜色、密度和熔点都可以在不改变物质性质的情况下观察到,所以这些都是锌的物理性质。