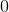例子问题
例子问题1:离子键
在离子键中,电子是__________.
可能的答案:
共享
转移
排斥
摧毁了
兴奋
正确答案:
转移
解释:
在离子键中,电子被转移形成化合物。例如,钠原子和氯原子可以结合,交换电子形成:
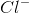

例子问题2:离子键
当离子键断裂时,这些分子中有哪些会形成?
可能的答案:
这些都不是;离子键永远不会分解。
阳离子
胶束
晶格结构
正确答案:
阳离子
解释:
离子键是指带相反电荷的离子之间相互吸引形成的键。离子化合物的一个例子是


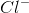
离子化合物有一种特殊的晶格结构,也就是说,离子以一种规则的几何模式排列。在



最后,胶束是脂质分子,它们在水溶液中呈球形排列。这是对脂肪酸有亲水性和疏水性区域(它们是两亲性的)这一事实的反应。它和离子键没有关系。
例子问题1:离子键
硫化铝的分子式是什么?
可能的答案:
正确答案:
解释:
硫的电负性比铝(一种金属)强得多,所以当它们结合时,铝将电子转移到硫上,它们就形成了离子化合物。铝的价电子是3,这意味着每个铝原子要共享或转移3个电子,以达到一个稳定的结构。硫的价是6,这意味着每个硫原子需要两个电子来完成它的八电子体。因此,两个铝原子将与三个硫原子成键,结果共转移了六个电子。
例子问题1:介绍主题
离子化合物氧化钠中阳离子的电荷是多少?
可能的答案:
正确答案:
解释:
当钠和氧形成离子化合物氧化钠时,
受欢迎的科目
丹佛的GMAT导师,波士顿的数学导师,费城的GRE导师,洛杉矶的物理导师,丹佛的微积分老师,洛杉矶的微积分导师,亚特兰大的ISEE导师,纽约市的代数导师,芝加哥的GRE导师,纽约市的GMAT导师