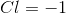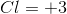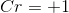例子问题
问题1:氧化还原反应
测定化合物中每个元素的氧化值
化合物中每个元素的氧化值
氯的氧化值是
因为这是中性原子,所以总电荷是0。因此我们可以
因此,
然后我们就能解出
问题5:反应
根据下式,确定还原剂。
回想一下还原剂被氧化并失去电子。因此,在看方程式的时候,要看哪个氧化态变得更正电。
首先给元素分配氧化态。
对于反应物:







现在,确定产物的氧化态。








只有
问题6:反应
在给定的反应中,哪些元素被氧化了?


让我们先来看看这个方程并根据已知的一般规则来分配氧化值:
让我们从反应物开始,也就是



接下来让我们看看




所以

现在我们有了反应物这边所有元素的氧化值。我建议把它们的氧化值一个接一个地写下来,这样就可以很快地确定被氧化和被还原的元素。
反应物中元素的氧化值:
现在我们来看看方程的生成物这边并确定这里元素的氧化值。首先让我们看看







最后,让我们看看



现在我们把产物中所有元素的氧化值写出来。
产品中元素的氧化值:
现在我们比较一下反应物和生成物中元素的氧化值。








问题7:反应
下面哪个化合物在a处有一个氮原子
首先,我们用已知的氧化态的基本规则逐个分析每个答案。在这个问题中最适用的规则是化合物中氢的氧化态通常等于

我们先来看看





解



不过,我们还是来看看其他情况:
因为这个化合物不带电荷我们知道它的净电荷等于
利用我们对氢和氧的氧化态的了解数一下这个化合物中氢和氧的个数,我们就能算出所有氢的总电荷等于

就像我们上面所做的那样,我们可以创建一个方程并解出未知数。
因此


接下来让我们看看
我们可以快速应用氧的氧化态知识知道化合物中氧的氧化态通常是



所以我们的方程变成了
因此

最后一个化合物是
对于这个化合物,我们可以应用我们知道的规则氢在化合物中的氧化态等于



因为有两个氮,我们的方程是:
和

问题1:分配氧化态
在下列化合物中,磷的氧化态最小?
首先,我们对已知的每种化合物逐一进行分析,并应用已知的氧化值的一般规律。
让我们从
我们知道,根据氧化态的一般规律,氧的氧化值通常是



现在我们可以解出磷的氧化态:
既然我们有



这个等于

解


接下来让我们看看
知道单质原子的氧化态是

现在让我们看看
知道氢的氧化值是


所以

现在让我们考虑一下
根据氧化值的基本规则,我们知道氧有



因此我们的方程是:
因此

最后让我们看看
使用上述规则
因此

这意味着氧化态最低的化合物是
问题2:分配氧化态
金的氧化态是什么
让我们首先考虑整个化合物






现在我们可以通过创建如下等式来求解金的氧化态:
化简后得到这个
问题3:分配氧化态
什么物质在接下来的化学反应中被还原?
还原被定义为获得电子,所以我们要找到获得电子/带负电的元素。
我们的方程是
我们从反应物这边开始
根据氧化态的一般规则,我们知道单质原子的氧化态等于零,因此

接下来,考虑



现在我们可以解出


现在让我们考虑一下
应用氧的氧化值规则
在哪里
这样就简化了

让我们考虑一下产品
我们知道氧的氧化态是


现在我们必须解出硫的氧化态:
因此

至于
观察生成物和反应物中元素氧化值的变化我们发现,在生成物和反应物中,硫,氢和氧的氧化态没有变化,但是铅从

问题4:分配氧化态
铜的氧化态是什么
为了确定铜在该化合物中的氧化态,我们首先必须注意到一个事实,即该化合物的总电荷为
我们也可以用已知的氧化值的一般规律来确定氢和氧的氧化值。因为氢是一个基团



至于氧,根据氧化值的一般规则,我们知道氧的氧化值通常是
因此

问题5:分配氧化态
硫的氧化值是多少
为了确定氧化值,我们必须应用已知的氧化值的一般规则。其中一条规则说氟的氧化值总是



这个方程是



因此,硫的氧化值为