例子问题
例子问题1:热力学系统与量热学
一位科学家正在为一堂化学课准备一个实验,以证明热力学第二定律。为了进行实验,科学家在一月份把全班同学带到室外,准备了一杯水和一个便携式炉子。
外面的温度是零下10摄氏度。科学家要求学生在回答他的问题时考虑以下问题:
吉布斯自由能公式:
Δg = Δh - tΔs
液固水相变反应:
H2O(l)⇌H2O(s) + X
科学家准备了两种场景。
场景1:
科学家把杯子埋在外面的雪里,和他的同学们一起回到教室一个小时,然后同学们检查杯子的情况。他们发现杯子里的水已经结冰了。
场景2:
然后,科学家把冰冻的一杯水放在炉子上,启动煤气。全班同学发现水融化得很快。
在水融化后,科学家要求学生考虑两个假设的场景作为思想实验。
场景3:
一旦场景2结尾的液态水完全融化,科学家就会关闭气体并监测水的变化。尽管在寒冷的空气中,水从来不会结冰。
场景4:
科学家从场景1的末端取下冻结的水,把它放在活跃的炉子上,水保持冻结状态。
在文章中描述的这种情况下,下列哪个选项是正确的?
一杯水是系统,炉子是环境。
一杯水是系统,而雪是环境。
一杯水就是系统,而雪、火炉和宇宙的其余部分就是环境。
系统是宇宙的全部,除了用来输入能量的炉子。
这个系统由一杯水、雪和炉子组成;宇宙就是周围的环境
一杯水就是系统,而雪、火炉和宇宙的其余部分就是环境。
吉布斯自由能方程利用了清晰描述的系统和环境。在这个例子中,水是结冰还是融化取决于条件。同时也伴随着与其他玩家的热量交换,如雪和炉子。因此,水是系统,而其他一切(严格来说,宇宙中的其他一切)构成了环境。
例子问题2:热力学系统与量热学
丙烷的燃烧由下式给出。
如果CO的生成热,CO2H2O和C3.H8分别为-110.5 kJ/mol, -393.5 kJ/mol, -241.8 kJ/mol, -103.85 kJ/mol,那么丙烷燃烧的反应热是多少?
-641.95 kj
-1477.9 kj
641.95 kj
1477.9 kj
-1477.9 kj
鉴于燃烧反应是放热,你应该期望反应热是负的(排除两个答案选择)。反应热等于生成物的生成热减去反应物的生成热。请务必参考配平的方程式,以确定每种化合物的正确摩尔数。
氧不包括在内,因为它是单质,因此它的生成热等于零。
例子问题1:热力学系统与量热学
液态己烷在298K时在空气中燃烧,生成气态二氧化碳和液态水,如反应所示。




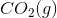


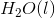

计算
计算

现在我们可以代入给定的值来解出反应的焓。
问题4:热力学系统与量热学
一个炉子要转移多少能量才能完全转化

为了把水变成蒸汽,炉子必须先提高水的温度,然后提供能量来改变相。这需要两个不同的步骤。
利用方程求出提高水温度的能量
现在,我们需要找出将水转化为气体所需要的能量。我们用这个方程
最后,我们将两步的能量相加,以求得所需的总能量。
例5:热力学系统与量热学
在上述反应中,74.0g硫与多余的氧气反应会释放多少热量?转到最近的10kJ。
基本上,这是一个单位转换问题。从硫的克数开始,转换为硫的摩尔数,最后转换为释放的热量的千焦。注意给定的反应焓,
注意,负的反应焓意味着这个过程是放热的并且释放热量,而正的反应焓意味着这个过程是吸热的并且吸收热量。
例子问题1:热力学系统与量热学
一种未知物质的50克样品被加热到100克oC在一盆沸水里。然后迅速取出,放入装有200毫升水的绝缘罐子中,初始浓度为20毫升oC.系统的最终平衡温度是30oC.这种未知物质的比热大约是多少?
水的比热为4.187J/goC。
水的密度为1g/mL。
由于系统是孤立的,从未知物质传递出去的热量一定等于传递给水的热量。计算这些热量,使用
为了水,
对于未知物质,
将这些值设为等于cx= 2.39 J/goC,大约2.4 J/goC。
问题61:生物化学,有机化学和其他概念
在-30的温度下改变一个50g的冰块需要多少能量oC放入50g水40oC ?根据需要使用上述数量,并四舍五入到最接近的kJ。
7 kj
22 kj
28 kj
17 kj
11 kj
28 kj
这种转变有三个不同的步骤:1)从零下30度加热冰oC到0oC, 2,在0点融化冰o3)从0开始加热水oC到40oC。
当温度发生变化时,我们使用

1)
2)
3)
把这三部分加起来就得到了总焓变,它等于能量的变化。
例8:热力学系统与量热学
哪个术语正确地描述了一个与周围环境有热交换,但没有物质交换的系统?
守恒的系统
封闭的系统
开放的系统
热力学系统
孤立系统
封闭的系统
在一个封闭系统中,能量和功可以与周围的区域交换,但物质是封闭的。例如,考虑一烧杯的冰。周围的热量转移到冰上,导致冰融化,但没有物质交换。没有任何外部化合物与冰反应,也没有任何冰离开烧杯。
在开放系统中,热和物质都可以交换。在孤立系统中,既不交换热,也不交换物质。
例子问题1:热力学系统与量热学
你开始一个实验


这个过程可以分为三个阶段:冰的温度升高,冰融化成水,水的温度升高。第一步和第三步使用物质的比热来计算所需的热量,而第二步使用熔合热。
第一步和第三步:
步骤2:
我们知道水的质量,温度的变化,以及常数值。使用这些值,我们可以将每一步所需的热量相加,从而得到最终答案。
例子问题10:热力学系统与量热学
根据需要对水使用以下值。
如果燃烧的木头释放



在这个问题中,有两个过程需要增加热量:
1.提高液态水的温度


2.把水以恒定的温度烧开

要使用这两个方程中的任何一个,我们需要用质量,密度和体积之间的关系来求出水的质量。
用这个质量和给定的比热和温度求出过程第一部分的热量。
然后,用给定汽化热的质量求出将水转化为水蒸气所需的能量。
将步骤1和步骤2的能量相加。
这是燃烧木材所需的总能量。用化学计量法求出产生这些能量所需的木头的克数。





















































































