例子问题
问题1:平衡常数和反应商
下列哪个关于K的陈述是错误的情商一个可逆的化学反应?
为K情商增加,反应中平衡产物浓度增加
在K中发现了纯液体和固体的浓度情商方程
K情商不受催化剂影响
K情商与温度有关吗
在K中发现了纯液体和固体的浓度情商方程
K情商只包括气体和水溶液的浓度。纯固体和纯液体的浓度不在方程中。
K情商由下式给出,其中表示的浓度为平衡浓度。
K情商是给定温度下给定反应的性质。催化剂只影响反应速率和活化能,不影响反应。等于K的值情商根据方程,增加,产物的平衡浓度也必须增加。
问题2:平衡常数和反应商
对于任何给定的化学反应,都可以画出能量图。能量图描述了反应中不同步骤的能级,同时也表明了能量的净变化,并提供了相对反应速率的线索。
下面是一个科学家在实验室里研究的反应图。一名学生在前一天晚上开始反应,但科学家不确定反应的类型。他找不到学生的笔记,除了下面的反应图。

最终,反应达到平衡。科学家改变了反应容器,再次测量了Q。他现在发现Q大于K的值情商他测量了反应达到平衡的时间。因为Q > K情商反应恢复平衡时必须克服的第一个活化能是多少?
第4点和第5点的能量差
点3和点4之间的能量差
点2和点3之间的能量差
点1和点2之间的能量差
点3和点5之间的能量差
第4点和第5点的能量差
因为Q现在大于K情商我们知道我们需要反向反应来回到平衡,此时Q = K情商。较大的Q值表明[产物]必须减少,以便在K处达到平衡情商。
在生成物到反应物的转化过程中,我们必须克服的第一个活化能是生成物的能量(第5点)和第一个过渡态(第4点)之间的差值。
问题3:平衡常数和反应商
写出给定反应的质量作用定律。
质量作用定律用于将化学方程与平衡常数进行比较。在方程式中,生成物的浓度在上面,反应物的浓度在下面。平衡方程中的系数变成平衡方程中的指数。虽然纯固体和液体可以排除在方程式之外,但纯气体仍然必须包括在内。
问题4:平衡常数和反应商
H的分压2和CH3.OH分别为0.5atm和1.4atm。反应平衡时CO的分压是多少?
要回答这个问题需要更多的信息。
如果反应处于平衡状态,我们知道质量作用定律等于上述信息中给出的平衡常数。当反应只包含气体时,分压值可以代替浓度。因此,我们只需要把这些值加到方程中,求解一氧化碳(CO)的分压。
问题5:平衡常数和反应商
一位科学家正在研究一种反应,并将反应物置于室温下的烧杯中。随着反应的进行,她通过核磁共振分析了产物。根据核磁共振读数,她确定反应过程如下:
为了更好地理解反应过程,她改变了反应物的浓度,研究了反应速率的变化。下表显示了她在三次实验中进行修改后的反应浓度。
当反应达到平衡时,下列哪一项是正确的?
反应物和生成物的能级是相等的
2正反反应的反应速率相等
3反应物和生成物的浓度是相等的
第三只
二只
II和III
I和II
I, II,和III
二只
当反应达到平衡时,正反反应速率相等。反应达到平衡状态与浓度无关。达到平衡也不会改变反应物和生成物固有的能量性质。
问题1:平衡常数和反应商
一位科学家正在研究一种反应,并将反应物置于室温下的烧杯中。随着反应的进行,她通过核磁共振分析了产物。根据核磁共振读数,她确定反应过程如下:
为了更好地理解反应过程,她改变了反应物的浓度,研究了反应速率的变化。下表显示了她在三次实验中进行修改后的反应浓度。
在某一特定时间点,上述反应的反应商计算为1.5。文中假设的特定条件下的平衡常数为0.06。关于反应平衡,下列哪个表述是正确的?
当反应达到平衡时,反应物的浓度将保持不变
当反应达到平衡时,反应物的浓度会增加
当反应达到平衡时,反应物的浓度会先升高,然后降低
当反应达到平衡时,反应物的浓度会先降低,然后升高
当反应达到平衡时,反应物的浓度会降低
当反应达到平衡时,反应物的浓度会增加
如果反应商大于平衡常数,则与平衡浓度相比,产物的相对丰度较高。反过来说,相对于平衡浓度,反应物一定是缺乏的。反应物的浓度需要增加,直到反应达到平衡。
问题1:平衡常数和反应商
这个反应的初始浓度列在下面。
根据这些初始浓度,哪个说法是正确的?
生成物与反应物之比大于平衡常数
反应处于平衡状态
反应会向左移动
远期汇率将大于反向汇率
远期汇率将大于反向汇率
当给定初始浓度时,我们可以确定反应商(Q)。反应商与平衡常数(生成物浓度除以反应物浓度)由相同的方程给出,但其值会随着系统反应而波动,而平衡常数则基于平衡浓度。
通过比较反应商和平衡常数,我们可以确定反应最初将朝哪个方向进行。
反应商和初始浓度写在下面。
这表明生成物与反应物之比小于平衡常数。因为Q小于K情商开始时,我们得出结论,反应会一直进行,直到Q等于K情商。这样,分母(反应物)减少,分子(生成物)增加,使Q更接近K情商。
问题1:平衡常数和反应商
一位科学家准备在化学课上演示热力学第二定律的实验。为了进行实验,这位科学家在一月份把全班学生带到室外,并收集了一杯水和一个便携式炉子。
外面的温度是零下10摄氏度。这位科学家要求学生在回答他的问题时考虑以下几点:
吉布斯自由能公式:
Δg = Δh - tΔs
液固水相变反应:
H2O(l) + H2O(s) + X
这位科学家准备了两种情景。
场景1:
科学家把杯子埋在外面的雪里,和他的学生一起回到教室,一个小时后,学生们检查杯子。他们发现杯子里的水已经结冰了。
场景2:
然后,科学家把冰冻的那杯水放在炉子上,启动煤气。全班发现水很快就融化了。
在水融化后,科学家要求学生们考虑两个假设的场景作为一个思想实验。
场景3:
一旦场景2结束时液态水完全融化,科学家就会关闭气体并监测水的变化。尽管处于寒冷的空气中,水却从不结冰。
场景4:
科学家从场景1的末尾取出冷冻的水,把它放在活动炉子上,水仍然是冷冻的。
文章中的同一位科学家测量了实验室中另一种反应的变量。他知道这个反应在标准条件下是自发的,标准自由能变化为- 43kj /mol。利用实验室计算的变量,他确定吉布斯自由能的值为0 kJ/mol。然后他计算了这个反应的反应商,同时知道平衡常数是3 × 103.。什么是正确的反应商?
它一定等于3 × 103.
它必须是零
它必须小于3 × 103.
一定是1
它必须大于3 × 103.
它一定等于3 × 103.
在平衡状态下,反应商和平衡常数相等。
问题9:平衡常数和反应商
对于任何给定的化学反应,都可以画出能量图。能量图描述了反应中不同步骤的能级,同时也表明了能量的净变化,并提供了相对反应速率的线索。
下面是一个科学家在实验室里研究的反应图。一名学生在前一天晚上开始反应,但科学家不确定反应的类型。他找不到学生的笔记,除了下面的反应图。

通道中的科学家能够计算出在容器中发生的反应的反应商(Q)。如果反应正在进行,但尚未达到平衡,反应商与反应常数(K情商)?
(假设反应在水溶液中进行,开始时有100%的反应物,没有生成物)。
K情商会小于Q吗
Q等于零,K等于情商会大于1吗
K情商Q等于
K情商等于0,Q大于1
Q小于K情商
Q小于K情商
在平衡态,K情商问题表明,从100%的反应物开始,反应还没有达到平衡。为了达到平衡,反应物必须不断减少,生成物必须不断积累。这就需要增加Q来最终达到K的值情商。本质上,Q从0开始,增加到K情商在平衡。
问题1:平衡常数和反应商
在上面的反应中,如果浓度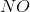
没有变化
对于一般的化学方程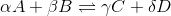
我们可以通过代入变量得到反应商方程。
注意浓度



![K_{eq}=\frac{[products]}{[reactants]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/85202/gif.latex)
![Q=\frac{[products]}{[reactants]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/132165/gif.latex)
![K_{eq}=\frac{[equilibrium\ product]}{[equilibrium\ reactant]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/85250/gif.latex)


![K_{eq}=\frac{[CH_3OH]}{[CO]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/30161/gif.latex)
![K_{eq} = \frac{[CO][H_{2}]^{2}}{[CH_{3}OH]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/30162/gif.latex)
![K_{eq} = \frac{[CH_{3}OH]}{[CO]2[H_{2}]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/30160/gif.latex)
![K_{eq} = \frac{[CH_{3}OH]}{[CO][H_{2}]^{2}}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/30159/gif.latex)
![aA+bB\rightarrow cC\ K_{eq}=\frac{[C]^c}{[A]^a[B]b}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/85996/gif.latex)
![CO(g) + 2H_{2}(g) \rightarrow CH_{3}OH(g)\ K_{eq}=\frac{[CH_3OH]}{[CO][H_2]^2}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/110360/gif.latex)









![\begin{matrix} Trial & [NH_4^+] & [NO_2^-] &Rate \\ 1& 0.480M &0.120M &0.018\frac{M}{s} \\ 2& 0.240M & 0.120M& 0.009\frac{M}{s}\\ 3& 0.240M& 0.360M & 0.027\frac{M}{s} \end{matrix}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/117028/gif.latex)

![\begin{matrix} Trial & [NH_4^+] & [NO_2^-] &Rate \\ 1& 0.480M &0.120M &0.018\frac{M}{s} \\ 2& 0.240M & 0.120M& 0.009\frac{M}{s}\\ 3& 0.240M& 0.360M & 0.027\frac{M}{s} \end{matrix}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/95871/gif.latex)


![[CH_{3}OH] = 2.5M, [CO] = 1.3M, [H_{2}] =0.6M.](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/115362/gif.latex)
![Q=\frac{[CO][H_2]^2}{[CH_3OH]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/183371/gif.latex)
![Q\ \text{or}\ K_{eq}=\frac{[CH_3OH]}{[H_2]^2[CO]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/183372/gif.latex)
![\frac{[2.5]}{[0.6]^{2}[1.3]} = 5.3](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/86003/gif.latex)
![Q=\frac{[products]}{[reactants]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/110330/gif.latex)
![K_{eq}=\frac{[equilibrium\ product]}{[equilibrium\ reactant]}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/85249/gif.latex)
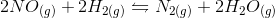




![Q=\frac{[C]^{\gamma}[D]^{\delta}}{[A]^{\alpha}[B]^{\beta}}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/668140/gif.latex)

![Q=\frac{[N_{2}][H_{2}O]^{2}}{[NO]^{2}{[H_{2}]}^{2}}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/668141/gif.latex)
![Q_2=\frac{[N_{2}][H_{2}O]^{2}}{[2NO]^{2}{[H_{2}]}^{2}}=\frac{[N_{2}][H_{2}O]^{2}}{4[NO]^{2}{[H_{2}]}^{2}}](https://vt-vtwa-assets.varsitytutors.com/vt-vtwa/uploads/formula_image/image/668142/gif.latex)




